台灣婦癌醫學會秘書長陳楨瑞醫師回憶,「因為肝臟轉移腫瘤,處理風險較高,與家屬討論之後,決定先做化學治療。經過數次化學治療之後,病人胸腔的肋膜積水完全消退,肚子裡面的腫瘤也縮小到能夠開刀的情況,才能安排手術把腹腔、骨盆腔裡的腫瘤切除。」
術後患者也繼續接受化學治療,陳楨瑞醫師表示,肝臟轉移的腫瘤也隨著化療而逐漸消失,患者的狀況也日漸改善。
除了化學治療外,患者更接受了基因檢測,並發現有BRCA-1基因突變,於是便向健保申請使用PARP抑制劑口服標靶藥物做維持性治療,希望可以維持在沒有復發的狀態。陳楨瑞醫師說:「能夠看到一位曾經被視為癌症末期、臥床的患者,在經過治療後,產生巨大轉變,實在是件令人高興的事。」
脹氣、腸胃不適,竟是卵巢癌
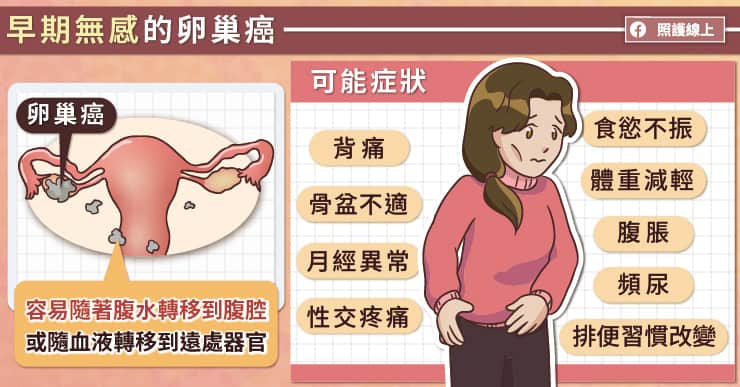
卵巢位於骨盆腔裡,形成腫瘤時,其實很難發現異狀,陳楨瑞醫師指出,隨著腫瘤變大,常見的症狀,包括脹氣、食慾不佳、體重降低或出現腹水,患者通常會在腸胃不適時而到腸胃科就診,被轉到婦產科才診斷出罹癌。
少數卵巢癌患者可能以陰道出血來表現,陳楨瑞醫師表示,停經後出血一般跟子宮內膜癌、子宮頸癌較有關係,但有少數卵巢癌患者,腫瘤侵犯到輸卵管或子宮,而造成陰道出血。
「卵巢癌可以長到相當大,達15-20公分以上,患者平躺時,能夠摸到肚子裡有不正常的腫塊。」陳楨瑞醫師說:「另外,癌細胞可能從肚臍的中間穿出來,嚴重的卵巢癌患者的肚臍甚至會長出腫塊。」
多元治療對抗卵巢癌
只要身體狀況許可,卵巢癌的治療大多會建議患者接受手術,陳楨瑞醫師分析,手術有兩個好處,第一是能夠取得足夠的組織來做病理檢驗,第二是能夠移除掉肚子裡絕大部分的卵巢癌。根據台灣的統計數據,五成以上的患者是屬於第三期卵巢癌,就是在腸壁、腹膜的表面有瀰漫性的癌細胞轉移,如果不把癌細胞清除乾淨,日後的化學治療容易產生較厲害的抗藥性,預後較差。除了手術外,八成到九成的卵巢癌的患者會接受化學治療。
隨著醫學發展,卵巢癌的治療也逐漸朝向個人化精準醫療邁進,透過基因檢測,能夠幫助患者找到適合的藥物。陳楨瑞醫師說,2015年有三位科學家,因為發現細胞的DNA修復機轉而榮獲諾貝爾化學獎。
同源重組修復基因是人體內參與DNA修復的重要基因,能協助維持細胞正常穩定生長,當這些基因發生突變或失能(同源重組修復缺失, 簡稱HRD)使得DNA無法準確地被修復,進而導致基因體的異常或不穩定,罹癌機率也因此提升。
其中同源修復機轉又與BRCA-1、BRCA-2,以及PARP最有關。陳楨瑞醫師解釋,體細胞具有雙股螺旋的修復機轉,癌細胞也有雙股螺旋修復機轉,所以我們可以使用干擾癌細胞修復機轉的藥物讓癌細胞凋亡。了解癌細胞基因突變的情況,有助於判斷患者對於藥物的反應,陳楨瑞醫師說,根據目前的治療準則,在建議上皮性卵巢癌的部分患者於接受手術後即考慮基因檢測。
PARP抑制劑標靶藥物有助延長存活期
陳楨瑞醫師表示:「患者接受化學治療後,癌細胞會受到傷害,導致DNA斷裂,這時癌細胞內的修復機轉便會啟動,而PARP就是一個單股DNA斷裂的修復因子。」如果能抑制PARP,某些癌細胞便無法修復損傷的DNA,它就沒辦法繼續分裂,而漸漸凋亡。
「雙股螺旋DNA修復機轉中最重要的兩個因子,一個是BRCA-1、另一個是BRCA-2, PARP則是修復單股DNA斷裂的重要因子。」陳楨瑞醫師解釋:「當患者具有BRCA突變的時候,代表體內修復雙股螺旋DNA損傷的能力有缺陷,如果再使用藥物來抑制負責修復單股DNA斷裂的PARP,就會增加DNA雙股螺旋斷裂的機會,癌細胞就會因為無法修復DNA損傷而凋亡。」
根據臨床研究,約20%的上皮卵巢癌患者為BRCA-1或BRCA-2基因突變,PARP抑制劑對於這類患者有顯著療效,而研究也顯示約半數上皮卵巢癌患者帶有同源重組修復缺失狀態(HRD),了解基因突變狀態有助於制定化療之後的維持性治療方式。陳楨瑞醫師說:「目前健保已有給付部分標靶藥物於晚期卵巢癌,作為維持性治療幫助延緩疾病復發」。
貼心小提醒
卵巢癌是種不容易察覺的癌症,超過五成的患者在發現時已是中後期卵巢癌,陳楨瑞醫師說,只要身體狀況許可,都建議要接受手術治療,盡量把腫瘤清除,同時要搭配化學治療、標靶治療等全身性治療。
透過個人化精準醫療,卵巢癌的治療成效已有顯著的進步,可以搭配基因檢測,了解本身基因突變狀態,後續配合標靶藥物做為維持性療法,延長存活期!
(本文獲「照護線上」授權轉載,原文刊載於此)